
Într-un articol am vorbit despre ce se întâmplă atunci când introducem sare în apă - de ce se dizolvă sarea în apă. Puteți citi articolul aici.
După cum să puteți observa dacă citiți cele două articole, cel de față și cel despre sare, dizolvarea zahărului în apă este diferită de cea a sării de bucătărie. Pe scurt, sarea este formată din ioni de clor (-) și de sodiu (+), care formează legături cu atomii de hidrogen, respectiv cu atomii de oxigen din moleculele de apă, astfel atomii din sare creând legături separate cu apa. Explicația pe larg o găsiți în articolul indicat.
În ce privește dizolvarea zahărului, iată ce se întâmplă...
Molecula de apă
Apa este un solvent, adică are capacitatea de a dizolva diverși compuși chimici, și este formată din doi atomi de hidrogen și un atom de oxigen.
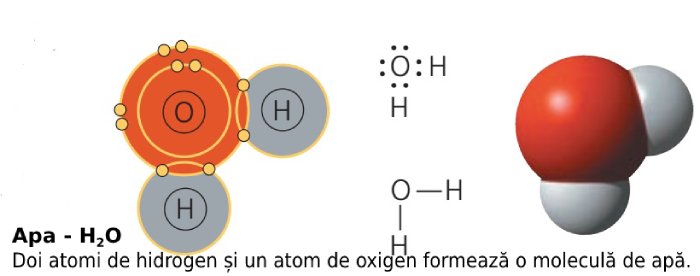
În cadrul moleculei de apă, ca urmare a cuplării atomilor de hidrogen la cel de oxigen, ultimul devine mai negativ, iar atomii de hidrogen vor avea o sarcină parțială pozitivă, având, așadar, o distribuție neuniformă a sarcinii în molecula de apă.
Având doi atomi cu sarcină electrică ușor diferită, vorbim despre o legătură polară. O explicație completă a electronegativității găsiți în articolul despre dizolvarea sării în apă.
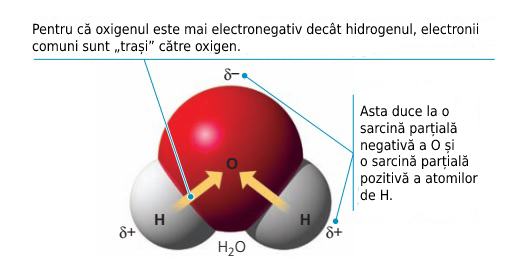
Datorită diferenței de sarcină, se formează o legătură între atomii de hidrogen ai unei molecule de apă și atomii de oxigen ai altei molecule de apă, legătură care se numește legătura de hidrogen, care este responsabilă de fluiditatea apei la temperatura camerei.
Cum se dizolvă zahărul în apă
Dacă sarea este un compus ionic (format din ioni), zahărul (sucroza, denumită și zaharoză) este un compus molecular.
Ce înseamnă asta? Că atunci când sucroza se dizolvă în apă, în fapt moleculele de sucroză rămân intacte, nu se „rup”, ca cele care formează sarea.
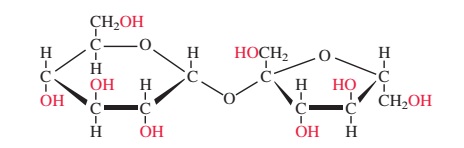
Structura chimică a sucrozei: C12H22O11
Dar cum are loc separarea moleculelor de sucroză? Ca urmare a atracției care are loc între moleculele de sucroză și moleculele de apă. După cum vedeți în imaginea de mai sus, în roșu, molecula de sucroză are 8 grupuri OH (oxigen-hidrogen).
Ce am explicat cu privire la sarcinile ușor diferite între atomii de oxigen și hidrogen la nivelul moleculei de apă este, desigur, valabil și în cazul grupurilor OH care fac parte din molecula de sucroză. Asta înseamnă că va exista o atracție între atomii de oxigen și cei de hidrogen dintre moleculele de apă și cele de sucroză.
Această atracție duce la separarea moleculelor de sucroză, deci, în final, la dizolvarea zahărului în apă.
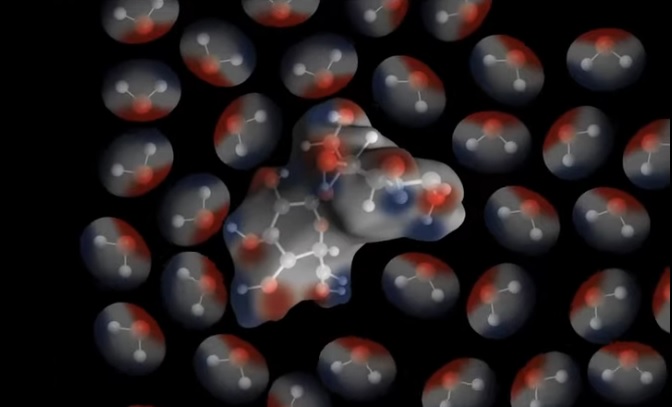
În imagine, în centru, vedeți molecule de sucroză, care sunt separate ca urmare a reacției cu moleculele de apă din jur.
Culoarea roșie arată sarcina mai negativă a oxigenului, iar albastrul sarcina mai pozitivă a hidrogenului.
Diferența de sarcină face ca atomii de oxigen și hidrogen de la moleculele de apă și sucroză să se atragă, astfel moleculele de sucroză se separă, având loc ceea ce numim dizolvarea zahărului în apă.
Atunci când apa este caldă, așa cum observă oricine bea un ceai ori o cafea cu zahăr, dizolvarea este mai rapidă, întrucât energia apei este mai mare, iar legăturile dintre moleculele de apă (legătura de hidrogen) sunt mai instabile.
În fapt, este nevoie de energie pentru a rupe legăturile dintre moleculele de sucroză, indiferent dacă apa este caldă ori rece. De asemenea, este nevoie de energie pentru a rupe legăturile de hidrogen dintre moleculele apă, care trebuie să fie anulate, pentru a introduce una dintre aceste molecule de sucroză în soluție. Zahărul se dizolvă în apă deoarece energia este emisă atunci când moleculele de sucroză, ușor polare, formează legături intermoleculare cu moleculele polare de apă.
Legăturile slabe care se formează între solut (substanța dizolvată) și solvent compensează energia necesară pentru a perturba structura atât a solutului pur, cât și a solventului.
În cazul zahărului și apei, până la 1800 de grame de sucroză se pot dizolva într-un litru de apă.
→ Citiți și: Ce este pH-ul unei substanțe? O explicație la nivel atomic.
Surse: cartea Campbel Biology, ediția a 10-a și acs.org
