Cu ceva timp în urmă am observat că mașina mea, 3 ani vechime, are semne de rugină la îmbinarea dintre un ornament și hayon. Fără măsuri, procesul de ruginire, pentru un obiect care stă afară, ca mașina, continuă nestingherit.
Dar ce se întâmplă atunci când ruginește o bucată de fier? Cum se transformă fierul în rugină? Iată, în continuare, o explicație la nivel atomic.
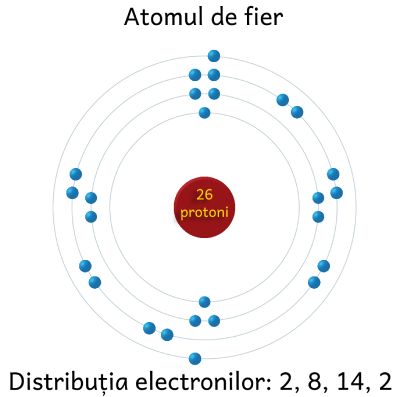
Fierul, după cum spune și numele, este format dintr-un singur tip de atom. După cum puteți vedea și în imaginea de mai sus, fierul are 26 de protoni (protonii dau identitatea unui atom; dacă se schimbă numărul de protoni, se schimbă și tipul de atom) și 26 de electroni, situați pe patru straturi energetice.
Notă: Imaginea de mai sus nu este o reprezentare fidelă a modului în care sunt distribuiți electronii în învelișul electronic al unui atom. Dacă nu sunteți familiarizați cu teoria modernă a atomului, citiți articolele noastre dedicate acestui subiect. În plus, în imagine nu sunt reprezentați protonii (26) și neutronii (30) care formează nucleul atomic.
Atunci când fierul ruginește, acesta formează o substanță maronie pe care o numim rugină. Această substanță are formula Fe2O3•xH2O. O să vedem în continuare cum se ajunge la această substanță.
Spre deosebire de alte metale care corodează, coroziunea fierului nu duce la formarea unei pelicule protective. Rugina se exfoliază continuu, expunând fierul procesului de ruginire.
Atât oxigenul, cât și apa sunt necesare pentru procesul de ruginire. Asta duce la aspecte aparent paradoxale:
- un cui de fier, introdus în apă neoxigenată, nu va rugini, chiar lăsat în soluție timp de săptămâni;
- un cui introdus în soluții care nu conțin apa, cum ar fi uleiul mineral, de asemenea, nu va rugini.
Procesul chimic al ruginirii
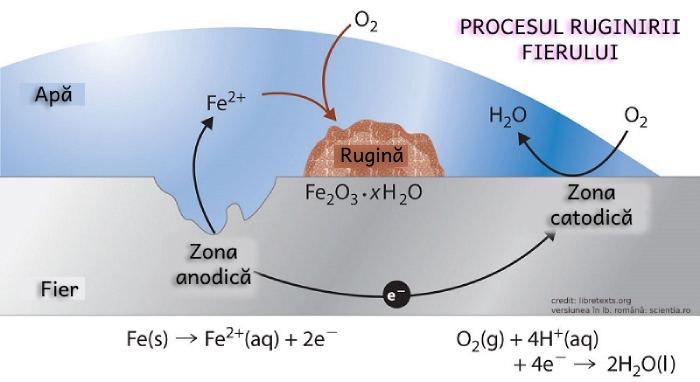
Procesul ruginirii
Pe scurt:
• undeva pe suprafața bucății de fier (zona catodică), oxigenul molecular (O2, din atmosferă) este redus la o moleculă de apă.
• în altă zonă, atomi de fier sunt oxidați (pierd 2 electroni) și devin Fe2+
• prima zonă devine un fel de catod, iar cea de-a doua - anod.
• cum s-a creat o diferență de potențial între cele două zone (anod și catod), electronii încep să se deplaseze în mod spontan de la anod către catod.
• apa acționează ca un solvent pentru Fe2+
• Fe2+ intră în reacție cu oxigenul atmosferic din apă și formează Fe2O3•xH2O.
Reacția care are loc la catod:
O2 + 4H+ + 4e− → 2H2O
Reacția care are loc la anod:
Fe → Fe2+ + 2e−
Fe2+ produs în reacția inițială este apoi oxidat de oxigenul atmosferic pentru a produce oxid hidratat care conține Fe3+:
4Fe2+ + O2 + (2+4x)H2O → 2Fe2O3•xH2O + 4H+
Probabil că lucrurile nu sunt foarte clare, așa că reluăm procesul cu o explicație mai detaliată.
O explicație de detaliu a procesului coroziunii fierului
• Ruginirea este, în fapt, procesul de revenire a fierului la forma sa inițială, de minereu de fier (Fe2O3).
• Luăm în calcul următoarea situație, ca în imaginea de mai sus: avem o bucată de fier, care intră în contact cu o picătură de apă. În continuare explicăm, pas cu pas, ce se întâmplă în procesul ruginirii, în acest context, al prezenței unei picături de apă pe suprafața unei bucăți de fier.
• Moleculele de oxigen (O2) din aer intră în interiorul picăturii de apă, având mai mare succes la o extremitate a picăturii de apă (nu în centrul ei).
• Când molecula de O2 atinge suprafața fierului (acest aspect are loc în partea dreaptă a imaginii de mai sus, zona catodică), aceasta ia doi electroni de la un atom de fier. Oxigenul are electronegativitate mare (adică „ține cu dinții” de electronii săi), dar preia „cu plăcere” electronii altor atomi, pentru a completa ultimul strat electronic (de la 6 la 8 electroni).
⇒ Citiți aici mai multe despre electronegativitate.
• Atomul de fier care tocmai a pierdut 2 electroni devine Fe2+ (plusul se referă la faptul că a deveni mai „pozitiv”, după pierderea electronilor).
• Dar acest ion de fier, care tocmai a pierdut electroni, nu are viață lungă. Electroni ai atomilor de fier din zona centrală a picăturii se deplasează (sub forma unui curent electric) către ionul de fier de la extremitate, aducând Fe2+ la forma sa inițială (Fe).
Așadar, atomii din regiunea centrală a picăturii devin Fe2+; aici, în fapt, în zona centrală, apare rugina!
• Ce s-a întâmplat cu O2 care a luat, inițial, doi electroni de la atomul de fier de la marginea picăturii de apă (zona catodică)? Devine un ion negativ, O2- (negativ, pentru că are un surplus de electroni, care sunt particule negative). Și imediat preia protoni de la ionii de H3O+ care se întâmplă să fie în vecinătate (acești ioni, H3O+, plus un hidroxid (OH-), apar în mod spontan în apă, din 2 molecule de apă (H2O)). În urma acestei „achiziții”, se formează molecule de apă. Așadar, pe scurt, oxigenul molecular (O2) „fură” electroni de la atomul de fier, iar apoi intră în reacție cu ionul hidroniu (H3O+) pentru a forma apă, H2O.
• Să ne întoarcem la ionii de fier (Fe2+) formați la centrul picăturii de apă (zona anodică). Aceștia se detașează de bucata de fier și sunt înconjurați de molecule de apă. Unde au fost ei, rămâne o mică gaură... Aventura transformării în rugină abia a început!
• Dar acești ioni de fier nu rezistă mult în acestă formă. Se lovesc de molecule de oxigen (O2) prezente în apă și mai pierd încă un electron, devenind Fe3+, iar molecula de oxigen molecular se rupe în doi ioni de O2-.
• Cum Fe3+ se formează chiar lângă ionii de O2-, aceștia se „cuplează”, date fiind sarcinile electrice diferite. Dar „capturează” în acest proces și molecule de apă, precum și diferite impurități prezente în apă. Acest conglomerat nou format este ceea ce numim rugină!
Reluând întregul proces, în cuvinte puține, procesul ruginirii constă în următoarele:
• atomii de fier pierd electroni către oxigenul molecular la suprafața fierului;
• ca urmare a acestei reacții are loc un transfer de electroni din altă zonă a suprafeței fierului către atomii de fier care tocmai au pierdut electroni;
• noii ioni de fier formați ca urmare a acestui transfer de electroni se desprind de bucata de fier, intră în reacție cu oxigen molecular și impurități din apă, formând rugina.
Înainte de a încheia, iată câteva aspecte bine de cunoscut despre fier:
• fierul este format în procesul de fuziune stelară, fiind cel mai greu element format astfel;
• se apreciază că este cel mai prezent atom din nucleul Pământului;
• atât plantele, cât și animalele au nevoie de fier.
Plantele - pentru a produce clorofilă, care este utilizată în fotosinteză (Cum funcționează fotosinteza).
Omul are nevoie de fier în hemoglobină, care are rolul de a transporta oxigen către celulele corpului.
Și unele bacterii au nevoie de fier, pentru fixarea azotului.
Surse:
• libretexts.org
• Cartea Reactions de Peter Atkins
