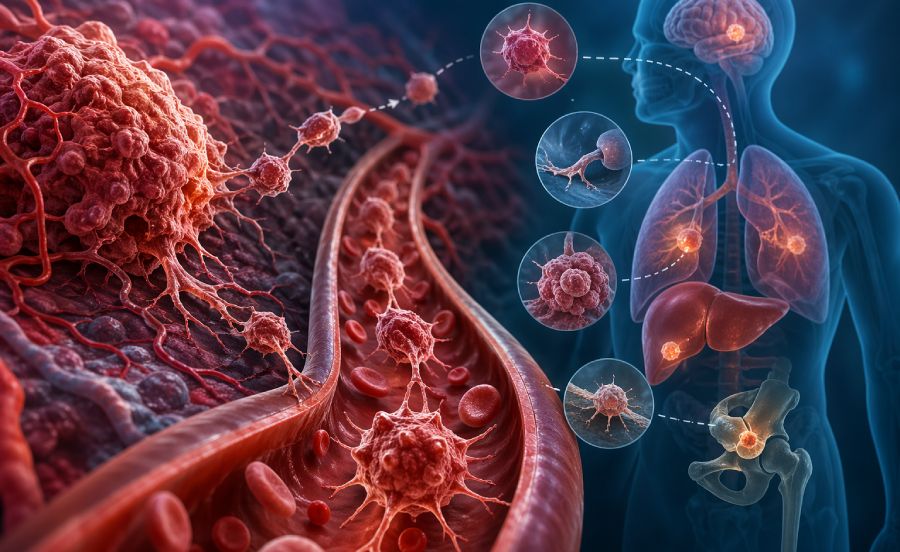
Înțelegerea acestor migrații uimitoare prin corpul uman, cunoscute sub numele de metastaze, ar putea sugera tratamente noi.
În 2014, o femeie cu cancer avansat a schimbat complet direcția cercetării științifice a lui Adrienne Boire. Cancerul, care începuse la nivelul sânului, ajunsese în lichidul cefalorahidian al pacientei, lăsând-o pe mama de vârstă mijlocie a doi copii incapabilă să meargă. „Când s-a întâmplat asta?”, a întrebat ea din patul de spital. „De ce cresc celulele acolo?”.
De ce, într-adevăr? De ce ar migra celulele canceroase în lichidul cefalorahidian, departe de locul în care au apărut, și cum reușesc să prospere într-un mediu atât de sărac în nutrienți?
Boire, medic și cercetător la Memorial Sloan Kettering Cancer Center din New York, a decis că aceste întrebări merită un răspuns.
Răspunsurile sunt urgente, deoarece ceea ce s-a întâmplat pacientei lui Boire se întâmplă unui număr tot mai mare de bolnavi de cancer. Pe măsură ce capacitatea de a trata tumorile inițiale sau primare s-a îmbunătățit, oamenii supraviețuiesc primelor etape ale bolii, doar pentru a reveni ani sau decenii mai târziu, când cancerul s-a reinstalat într-un alt țesut, cum ar fi creierul, plămânii sau oasele.
Acesta este cancerul metastatic, principalul responsabil pentru decesele prin cancer. Deși cifrele precise sunt greu de stabilit, între aproximativ jumătate și o mare majoritate a deceselor cauzate de cancer sunt atribuite metastazelor. Oferirea unor opțiuni și speranțe mai mari pacienților va depinde de înțelegerea modului în care aceste celule reușesc să migreze și să recolonizeze alte țesuturi.
Prevalența metastazelor ascunde dificultatea enormă a călătoriei pe care celulele canceroase trebuie să o parcurgă.
O celulă apărută, de exemplu, în sân este bine adaptată să trăiască acolo: să utilizeze acizii grași disponibili, să reziste amenințărilor locale și să crească într-o tumoră solidă. Dacă reușește să pătrundă în fluxul sanguin, se deplasează cu viteze de până la 40 de centimetri pe secundă, fiind supusă unor forțe de forfecare suficiente pentru a o distruge. Dacă supraviețuiește acestei călătorii și ajunge într-un alt țesut, de exemplu creierul sau lichidul cefalorahidian, mediul este complet diferit. Nutrienții cu care era obișnuită pot lipsi, iar celulele sistemului imunitar sau alte molecule din mediu o pot ataca. Pentru ca o celulă să reușească această deplasare și apoi să se adapteze, este o sarcină cu adevărat herculeană.
„Nu este deloc simplu sau banal”, spune Ana Gomes, biolog specializat în cancer la Moffitt Cancer Center din Tampa, Florida. „Este contrar a tot ceea ce ține de natura acestor celule.”
Migrarea către un nou loc și formarea unei noi tumori reprezintă un proces dificil pe care puține celule îl finalizează. O celulă trebuie să părăsească tumora inițială, să supraviețuiască în sânge și să pătrundă într-un nou țesut. Chiar și atunci, celula poate rămâne o perioadă în stare latentă, până când mediul permite diviziunea și creșterea ei pentru a forma o nouă tumoră.
Nu este surprinzător că, deși tumorile eliberează în mod regulat celule, majoritatea celor care scapă mor sau rămân inactive fără a se stabili ca metastaze. „Personal, cred că metastaza este un accident”, spune Matthew Vander Heiden, medic-cercetător și director al Koch Institute for Integrative Cancer Research de la MIT. „Este un proces extrem de ineficient.”
Puținele celule care reușesc această performanță sunt rezistente și flexibile în modul în care își obțin energia și procesează moleculele din jur. Ele își pot modifica biochimia pentru a evita pericolele locale sau pentru a obține combustibil într-un mediu sărac. Unele chiar trimit semnale înainte pentru a modifica organul în care vor ajunge, pregătind un mediu favorabil, cu resurse disponibile la sosire. „Modificările metabolice ajută aceste celule să facă față tuturor acestor provocări”, spune Patricia Altea-Manzano, cercetător biomedical la Centrul Andaluz de Biologie Moleculară și Medicină Regenerativă din Sevilla, Spania.
Astfel de descoperiri sugerează că celulele metastatice, fiind atât de diferite de tumora originală, ar putea fi vulnerabile la noi tipuri de tratament. În viitor, medicii ar putea interveni înainte ca metastazele să se stabilească pentru a bloca sau încetini răspândirea cancerului. „Aceasta este o oportunitate foarte mare”, spune Gomes.
Adaptări noi
Din punct de vedere metabolic, nu există loc mai bun decât cel de origine: cancerele tind să se dezvolte cel mai bine în țesuturile în care au apărut inițial, a constatat grupul lui Vander Heiden. De asemenea, atunci când migrează, aceste tumori primare au preferințe pentru anumite locuri-țintă; de exemplu, cancerul de prostată metastazează frecvent în oase.
Totuși, unele celule ajung în locuri în care este foarte puțin probabil să se poată adapta. Anumite țesuturi, precum splina și mușchii scheletici, par să reziste metastazelor, iar motivele sunt multiple. Celulele musculare, de exemplu, consumă cantități mari de energie, determinând mitocondriile să elibereze cantități mari de specii reactive de oxigen, cum ar fi peroxidul de hidrogen. Aceste molecule puternic oxidante sunt toxice, dar celulele musculare le pot gestiona. În schimb, deși numeroase celule tumorale ajung în mușchii scheletici prin fluxul sanguin abundent, ele rareori reușesc să se stabilească acolo, probabil din cauza acestor molecule reactive.
Adaptarea la alte medii este însă posibilă. Vander Heiden a demonstrat acest lucru când echipa sa a implantat celule umane de cancer mamar fie în țesutul adipos mamar, fie în creierul șoarecilor. Deși creierul nu conține acizii grași pe care aceste celule sunt obișnuite să îi utilizeze, atunci când au fost plasate în creier, ele s-au adaptat și au început să își producă propriii acizi grași.
Cercetătorii au tratat apoi șoarecii cu un medicament care blochează sinteza acizilor grași, iar celulele canceroase din creier au crescut la jumătate din ritmul obișnuit (în timp ce cele din țesutul mamar nu au fost afectate). Vander Heiden a colaborat cu companii care explorează această abordare ca posibil tratament.
Uneori, tumorile pot chiar să pregătească un loc străin înainte de sosire, într-un proces numit de unii cercetători „educarea nișei metastatice”. Cancerele eliberează nu doar celule, ci și hormoni, ADN și mici vezicule lipidice în sânge și limfă. Aceste vezicule conțin mesaje chimice care, odată ajunse în organe îndepărtate, pot remodela țesuturile în favoarea celulelor tumorale. Această „educare” ajută celulele metastatice să prospere în noul mediu, spune Gomes.
Chiar și microbii pot contribui la acest proces. În cazul cancerului colorectal, bacteriile intestinale pot „învăța” ficatul să accepte celule canceroase metastatice. Aceste bacterii colonizează tumora intestinală, traversează bariera care separă conținutul intestinal de restul organismului și ajung în ficat, unde induc inflamație. Aceasta creează un mediu favorabil tumorilor, permițând celulelor canceroase să se stabilească.
Legătura cu acizii grași
Altea-Manzano a studiat acest proces de „pregătire” în perioada sa ca cercetător postdoctoral, lucrând împreună cu biologul specializat în cancer Sarah-Maria Fendt la VIB-KU Leuven Center for Cancer Biology din Belgia. În acest caz, plămânii erau cei „pregătiți” de tumori aflate în alte părți ale organismului. Și, la fel cum a observat Vander Heiden în cazul metastazelor cancerului mamar la creier, accesul la acizi grași a fost un factor-cheie - în mod concret, acidul gras palmitat, ale cărui funcții includ rolul de sursă de energie și de componentă a membranelor celulare.
Plămânii sunt deja bogați într-un material bogat în lipide numit surfactant, care acoperă interiorul acestora și împiedică colapsul țesutului pulmonar. Atunci când cercetătorii au hrănit șoarecii cu o dietă bogată în grăsimi, nivelurile de palmitat și de alți acizi grași din plămâni au crescut. Iar când cercetătorii au injectat în sângele acestor șoareci celule de cancer mamar provenite de la șoarece, dieta bogată în grăsimi a dus la o creștere de peste două ori a metastazelor pulmonare.
Pentru a verifica dacă celulele tumorale secretă substanțe care pregătesc plămânii să le găzduiască, Altea-Manzano și colaboratorii au cultivat fragmente de tumori mamare de șoarece într-un vas de laborator, apoi au colectat lichidul care conținea toate secrețiile celulare. Când au injectat acest lichid lipsit de celule la șoareci, nivelul de palmitat din plămâni a crescut; dacă au injectat și celule canceroase, acest tratament a crescut și nivelul metastazelor pulmonare produse de aceste celule. O anumită componentă produsă de celulele canceroase cultivate în acel vas de laborator transmitea plămânilor un semnal: produceți mai mult palmitat. (Cercetătorii nu sunt încă siguri care este substanța de semnalizare.)
Rezultatul este că, dacă o celulă de cancer mamar ajunge în plămâni, găsește un „ospăț” bogat în lipide, deja pregătit. Pentru a valorifica acest nou „meniu”, însă, o celulă de cancer mamar recent ajunsă trebuie să își modifice biochimia celulară. Ea face acest lucru modificându-și mitocondriile, astfel încât acestea să poată prelua mai mult palmitat. În experimentele pe șoareci, blocarea acestei modificări a împiedicat metastazarea, indiferent de cantitatea de palmitat disponibilă. Același lucru s-ar putea întâmpla și la pacienții umani, speculează Altea-Manzano, care, împreună cu Fendt și alți cercetători, a fost coautor al unei analize privind modificările metabolice ce ar putea favoriza sau împiedica metastazarea, publicată în ediția din 2024 a Annual Review of Cancer Biology.
Cunoașterea adversarului
Pe lângă locurile bogate în lipide, precum plămânii, cancerele se pot adapta unor medii surprinzător de dificile, cum este mediul extrem de sărac reprezentat de lichidul cefalorahidian care înconjoară creierul și măduva spinării.
Majoritatea locurilor din organism în care apar tumorile sunt bogate în nutrienți: lipide, aminoacizi, oxigen, metale — toate substanțele necesare unei celule aflate în creștere rapidă. În schimb, „creierul este un fel de prințesă metabolică”, spune Boire. „Preferă doar glucoză.”
Nu doar că există foarte puține resurse nutritive, dar celulele canceroase se află și înconjurate de celule de susținere ale sistemului nervos și de celule imunitare rezidente, ambele eliberând factori cu efect antitumoral.
Activitatea lui Boire se concentrează asupra lichidului cefalorahidian. Acesta este un lichid limpede, lipsit de multe dintre substanțele nutritive, și totuși metastazele în lichidul cefalorahidian apar la aproximativ 5% până la 10% dintre pacienții cu tumori solide și, de regulă, duc la deces în câteva luni. Pentru Boire, acest tip de cancer reprezintă „un adversar redutabil … este complet malign”.
Pentru a înțelege cum supraviețuiește o astfel de celulă, Boire și colaboratorii au analizat celule metastatice provenite de la cinci pacienți la care cancerul de sân sau de plămân invadase lichidul cefalorahidian. Toate aceste celule își intensificaseră un sistem biochimic care captează fierul, un metal esențial pentru producerea de energie și pentru sinteza componentelor celulare. Ca parte a acestui sistem, celulele secretau o proteină numită lipocalina-2, care colectează fierul puțin disponibil din mediul înconjurător; în paralel, produceau o altă proteină, un transportor lipocalină-2–fier, care introduce în celule complexul format din fier și lipocalina-2.
Puncte vulnerabile
Pe lângă nutrienți, celulele canceroase aflate în migrație au nevoie de protecție împotriva modificărilor metabolismului lor în noile medii. Procesul de metastazare în sine pare să determine celulele canceroase să genereze specii reactive de oxigen, care le pot distruge din interior, spune Sean Morrison, biolog specializat în cancer la University of Texas Southwestern Medical Center din Dallas. Echipa sa studiază acest obstacol al metastazării injectând celule umane de melanom la șoareci. Cercetătorii pot introduce celulele chiar sub piele, unde ar trebui să fie într-un mediu favorabil, sau le pot injecta în alte locuri, precum fluxul sanguin sau splina, pentru a vedea dacă pot realiza metastaze. În piele, celulele de melanom nu sunt supuse unui stres oxidativ semnificativ. Însă celulele de melanom din sânge sau din alte organe sunt supuse unui stres cauzat de niveluri mai ridicate de specii reactive de oxigen. Este posibil ca nivelurile mai mari de fier și oxigen din locuri precum sângele să determine modificări biochimice care duc la producerea acestor molecule periculoase, sugerează Morrison.
Stresul oxidativ distruge celulele de melanom aflate în migrație printr-un proces numit ferroptoză, în care acizii grași polinesaturați din membrana celulei canceroase reacționează cu fierul. „Este ca un incendiu de grăsime care pornește în celulele canceroase în timp ce încearcă să migreze”, spune Morrison.
Totuși, unele celule de melanom dobândesc un mecanism de apărare dacă traversează mai întâi sistemul limfatic înainte de a se stabili într-un țesut. În limfă, membranele lor acumulează acizi grași mononesaturați, care nu reacționează cu fierul în același mod, ajutându-le să reziste ferroptozei, au raportat cercetătorii.
Și aceasta nu este tot. Celulele de melanom care au fost cele mai eficiente în metastazare și-au reconfigurat metabolismul, au descoperit oamenii de știință. Ca urmare, ele au consumat în cantități mari o moleculă numită lactat din mediul înconjurător și par să utilizeze acest lactat pentru a produce molecule protectoare, cu rol antioxidant. Atunci când cercetătorii au blocat capacitatea celulelor de melanom de a absorbi acest lactat, boala metastatică la șoareci a fost redusă.
În schimb, atunci când au tratat șoarecii cu cantități suplimentare de antioxidanți, celulele aflate în metastazare au avut o probabilitate mai mare de a supraviețui în fluxul sanguin și în alte organe; la unii dintre șoarecii tratați, numărul celulelor metastatice care circulau prin sânge s-a mai mult decât dublat.
Acest rezultat, publicat în 2015, a fost o surpriză majoră, spune Morrison: „Oamenii consideră antioxidanții ca fiind benefici pentru sănătate.” În cazul șoarecilor din laboratorul său, însă, antioxidanții au fost benefici și pentru celulele canceroase, foarte benefici. Publicația The Washington Post a descris studiul drept „înfricoșător”, „provocator” și „alarmant”.
Într-un experiment, cercetătorii au studiat o linie de șoareci la care fusese injectat melanom sub piele. Tratamentul cu un antioxidant a crescut semnificativ proporția celulelor din sânge care erau celule de melanom metastatice (stânga), precum și încărcătura — adică cantitatea — de celule canceroase metastatice din organele interne (dreapta).
Totuși, aceste rezultate sunt în concordanță cu studii anterioare privind antioxidanții la pacienții cu cancer. În cercetări desfășurate de-a lungul mai multor decenii, antioxidanți precum beta-carotenul și vitamina E au fost asociați cu creșterea incidenței cancerului pulmonar și a mortalității la fumători, precum și cu o incidență mai mare a cancerului de prostată la bărbați sănătoși. Deși aceste studii nu s-au concentrat asupra cancerului metastatic, Morrison consideră că există o legătură. „Realitatea este că, în anumite faze-cheie ale evoluției cancerului, celulele canceroase sunt foarte aproape de a muri din cauza stresului oxidativ, astfel încât beneficiază mai mult de pe urma antioxidanților decât celulele normale”, speculează el.
Dacă antioxidanții pot favoriza cancerul, atunci creșterea nivelului de specii reactive de oxigen ar putea combate anumite tipuri de metastaze. Într-adevăr, unele tratamente oncologice actuale amplifică producția de specii reactive de oxigen pentru a distruge celulele canceroase.
Aceste rezultate sugerează că alegerile alimentare sau suplimentele ar putea influența riscul de cancer și de metastazare. De exemplu, Morrison speculează că o dietă bogată în acizi grași polinesaturați ar putea duce la o cantitate mai mare de astfel de acizi grași pro-ferroptoză în membranele celulelor canceroase. Dacă celulele sunt deja vulnerabile, o cantitate suplimentară de grăsimi polinesaturate ar putea fi încă un factor care le împinge spre moarte celulară. Pentru o dată, aceasta ar fi o dietă ușor de urmat: un exemplu de preparat ar putea fi somon prăjit în ulei de soia, sugerează Morrison.
Modificarea dietei nu va elimina cancerul de una singură, spune Fendt. Totuși, adaugă ea, ar putea încetini progresia bolii sau ar putea ajuta alte tratamente să funcționeze mai bine — deși, așa cum arată studiile privind antioxidanții, efectele dietei pot fi dificil de anticipat.
„Este important să avem dovezi științifice foarte solide și riguroase pentru aceste întrebări”, avertizează Fendt. Unele studii sunt în desfășurare, însă, în prezent, nu există o dietă „anti-metastază” care să poată fi recomandată.
Traducere după How cancer cells travel to new tissues and take hold de
Traducerea nu preia imaginile din articolul original.
This article originally appeared in Knowable Magazine, a nonprofit publication dedicated to making scientific knowledge accessible to all. Sign up for Knowable Magazine’s newsletter.
