 Dacă lumina manifestă în anumite circumstanţe proprietăţi corpusculare, oare în cazul particulelor elementare, precum electronii sau protonii am putea vorbi de un comportament similar undelor? Fizicianul francez Louis de Broglie oferă un prim răspuns atunci când îşi susţine teza de doctorat, în 1924.
Dacă lumina manifestă în anumite circumstanţe proprietăţi corpusculare, oare în cazul particulelor elementare, precum electronii sau protonii am putea vorbi de un comportament similar undelor? Fizicianul francez Louis de Broglie oferă un prim răspuns atunci când îşi susţine teza de doctorat, în 1924.
Ipoteza lui de Broglie
În cadrul tezei sale de doctorat, prezentată în 1923, fizicianul francez Louis Victor de Broglie, un tânăr născut la 15 august 1892 într-o familie nobiliară originară din Piemont, Italia, formulează o ipoteză foarte curajoasă, şi anume ideea că particulele considerate la vremea respectivă corpusculi de materie (de exemplu electronii), au o natură duală, corpusculară şi ondulatorie, asemenea radiaţiei electromagnetice. Louis de Broglie primeşte Premiul Nobel pentru teza sa de doctorat în anul 1929.

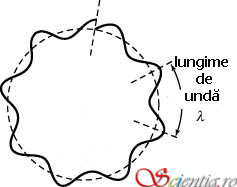
De Broglie asociază o undă de o anumită frecvenţă fiecărei particule, oprindu-se în mod special la descrierea naturii duale a electronului. Francezul propune şi o formulă de calcul a lungimii de undă asociată unei particule elementare, în funcţie de impulsul (deci viteza şi masa) particulei. Desigur, şi constanta lui Planck joacă un rol în ecuaţia propusă de Louis de Broglie: λ=h/p, unde p=mxv. Lungimea de undă asociată materiei poartă numele de lungime de undă de Broglie.
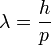
Semnificaţia constantei lui Planck
Problematica dualismului particulă-undă. Fragment dintr-un documentar BBC Two
Studiind formula propusă de Louis de Broglie pentru descrierea “undelor de materie”, cum sunt denumite undele asociate materiei propuse de francez, se observă că dacă lumea microscopică nu ar prezenta acest caracter granular, fapt echivalent matematic cu o valoare nulă asociată constantei lui Planck, atunci şi lungimea de undă propusă de Louis de Broglie ar deveni 0 (dacă h->0, atunci λ->0), anulând aspectul ondulatoriu al particulelor elementare.
Altfel spus, mecanica cuantică, redusă la ideea centrală că există o limită minimă, nenulă, până la care poate fi divizată energia, limită stabilită de valoarea constantei lui Planck, sugerează în mod indirect în contextul formulei propuse de Louis de Broglie natura ondulatorie a constituenţilor fundamentali ai materiei şi, în consecinţă, existenţa unei unde asociate lor.
Putem vorbi de unde de materie şi în cazul obiectelor macroscopice?
Există fizicieni care susţin că răspunsul la întrebarea de mai sus este da. Cel puţin în principiu. Numai că, aşa cum sugerează formula lui de Broglie, în cazul obiectelor macroscopice ordinul de mărime al masei acestora generează lungimi de undă care tind spre valoarea zero (dacă m este foarte mare, atunci λ->0). Pe de altă parte, comportamentul ondulatoriu al unui obiect se manifestă şi devine observabil la interacţiunea sa cu un sistem de dimensiuni comparabile cu lungimea sa de undă.
Aşadar, la nivel macroscopic, lungimile de undă asociate obiectelor sunt prea mici pentru a produce efecte observabile. În schimb, pentru cazul electronului, formula lui de Broglie furnizează o lungime de undă asociată comparabilă cu dimensiunile sistemelor cu care electronul interacţionează în mod natural, şi anume constituenţii atomilor. Ceea ce înseamnă că în cazul electronilor natura lor ondulatorie ar trebui să creeze efecte observabile cu ajutorul anumitor montaje experimentale.
Ca o concluzie, aspectele ondulatorii ale materiei devin observabile pentru particulele elementare, şi nicidecum în cazul structurilor macroscopice.
O excepţie – structurile macroscopice aflate la temperaturi apropiate de 0 K.
Ce se întâmplă însă cu structurile macroscopice dacă viteza din formula lui de Broglie este nulă? În context macroscopic, viteza din formula lui de Broglie este de fapt un indicator al agitaţiei termice a sistemului (nu vorbim de viteza de deplasare a unui anume obiect, ci de viteza unui sistem macroscopic prin prisma energiei de mişcare a constituenţilor fundamentali ai sistemului). Se ştie din teoria cinetică a gazelor că scăderea agitaţiei termice a unui sistem, adică reducerea spre zero a mişcării (vitezei) particulelor constituente, se poate obţine prin scăderea drastică a temperaturii respectivului sistem. În mod ideal, energia (deci viteza) sistemului macroscopic poate fi redusă la o valoare aproximativ nulă doar în condiţiile în care sistemul este răcit la temperaturi foarte apropiate de zero absolut.
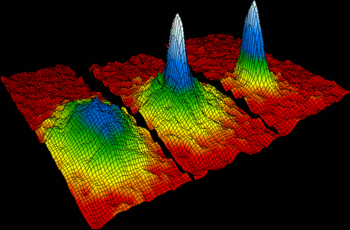
Credit: wikimedia.org
Acum câţiva ani s-a reuşit acest lucru obţinându-se în laborator aşa-numitul condensat Bose-Einstein, un gaz foarte dens din atomi aduşi aproape de 0 K. Cum undele de materie asociate acelor atomi au lungimi de ordine de mărime comparabile cu distanţele dintre atomi, undele respective încep să “se simtă” reciproc, coordonându-şi starea şi ducând la apariţia unui “superatom”, un sistem complex descris de o funcţie de undă asociată lui. Aşadar, fizica temperaturilor foarte scăzute este un domeniu care poate fi folosit pentru a pune în evidenţă unele dintre predicţiile mecanicii cuantice.
Când au apărut primele dovezi experimentale în sprijinul ipotezei lui Louis de Broglie?
Confirmarea experimentală a existenţei “undelor de materie” vine în anul 1927 de la fizicienii americani Clinton Davidsson şi Lester Germer. Aceştia au pus în evidenţă pe cale experimentală difracţia unui fascicul de electroni la contactul cu un cristal de nichel, prima situaţie când sunt observate caracteristici similare undelor în cazul electronilor. George G.P. Thomson a reuşit acelaşi lucru ulterior folosind un film fotografic din celuloid şi apoi şi alte materiale. Davisson şi Thomson şi-au împărţit Premiul Nobel în 1937 pentru „descoperirea fenomenelor de interferenţă care se produc când cristalele sunt expuse acţiunii unor fascicule de electroni”.

Clinton Davidsson şi Lester Germer
Credit: rpi.edu
În 1961, Claus Jönsson a reuşit pentru prima dată punerea în scenă a celebrului experiment al lui Thomas Young, folosind însă electroni (nu fotoni, ca în original) şi observând apariţia fenomenului de interferenţă, pentru ca în 1989 Akira Tonomura şi colegii săi de la Hitachi să pună în evidenţă franjele de interferenţă folosind o sursă foarte slabă de electroni (trimiţând practic rând pe rând câte un electron spre o biprismă).
Ce progrese a adus ipoteza lui de Broglie în mecanica cuantică?
Dincolo de ideea lui de Broglie, revoluţionară în sine, ipoteza francezului a oferit o modalitate nouă de a interpreta teoria atomică pe care Niels Bohr a formulat-o în 1913. Bohr a descris electronii drept particule care aveau orbite fixe, iar modelul vizual asociat atomului său este utilizat şi astăzi pe scară largă. Modelul atomic al lui Niels Bohr se baza însă pe câteva ipoteze, printre care şi faptul că electronii pot orbita numai la anumite distanţe de nucleu, ipoteze pentru care Bohr nu a oferit nicio justificare.
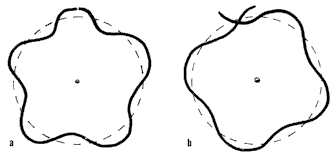
Orbită electronică permisă (stânga), respectiv interzisă (dreapta) de teoria lui Louis de Broglie
Asociind electronilor proprietăţi ondulatorii, de Broglie schimbă modelul vizual al lui Bohr, reprezentând electronul ca o undă circulară. La absorbţia unui foton, o undă adiţională este încorporată, ceea ce rezultă fiind trecerea electronului pe o orbită superioară (lungimea respectivei „corzi” vibrante circulare creşte prin înglobarea unui foton). Postulatul lui Bohr, deci faptul că orbitarea poate avea loc doar la anumite distanţe de nucleu, poate fi explicat astfel: doar orbitele care conţin pe toată circumferinţa lor un număr întreg de lungimi de undă sunt permise. Observaţi în imaginile de mai jos despre ce este vorba:
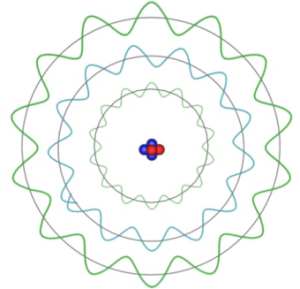
O animaţie sugestivă poate fi văzută aici !
Dualitatea particulă-undă în contextul interpretării Copenhaga

Bohr a extins ideea dualismului corpuscul-undă formulând un principiu al complementarităţii, care spune că cele două aspecte sunt complementare, iar nu contradictorii. Conform acestui principiu, a te întreba care este adevărata natură a unei particule fundamentale este o eroare de logică. Pentru a observa comportamentul electronului este necesar un anumit experiment care, susţine Bohr, scoate la iveală doar una dintre faţetele electronului. O analogie superbă este cea cu o monedă. Un experiment care îşi propune să studieze electronul poate fi asemănat cu “datul cu banul”. La final, nu poţi vedea decât fie capul, fie pajura, nicidecum pe ambele.
Aplicaţii. Microscopul electronic
Una dintre cele mai importante aplicaţii practice care se folosesc de aspectul ondulatoriu al electronilor este microscopul electronic. Nu vom detalia aici tehnologia din spatele acestei extraordinare invenţii. Vom prezenta în schimb principiul teoretic care permite funcţionarea acestui aparat.

Imaginea unei furnici obţinută cu un microscop electronic
Credit: wikimedia.org
Fineţea de percepţie a microscoapelor este strâns legată de lungimea de undă a razelor cu care se “iluminează” obiectul studiat. Cu cât lungimea de undă a acestora este mai mică, cu atât rezoluţia obţinută creşte. Dacă ne raportăm la formula lui de Broglie (λ=h/p) şi facem o comparaţie între fotoni şi electroni, rezultă în mod clar faptul că undele de materie asociate electronului au lungimi de undă mai mici decât cele ale luminii vizibile. Pentru undele electromagnetice din spectrul vizibil lungimea de undă este în zona 400-800 nm, în timp ce undele asociate electronilor folosiţi în microscoapele electronice moderne au valori mai mici de 1pm. Astfel, anumite microscoape electronice ajung să mărească de 2 milioane de ori, pe când cele mai bune microscoape optice măresc de doar 2 000 de ori.
Bibliografie:
Paul Davies and John Gribbin - The matter myth
physicsworld.com/cws/article/print/9745
nobelprize.org/nobel_prizes/physics/laureates/2001/public.html
www.sanatatea.com/art/savanti/2316-louis-victor-de-broglie.html
ro.wikipedia.org/wiki/Microscop_electronic
www.sr.bham.ac.uk/xmm/atom1.html
www.youtube.com/watch?v=oUolVZIuv18
