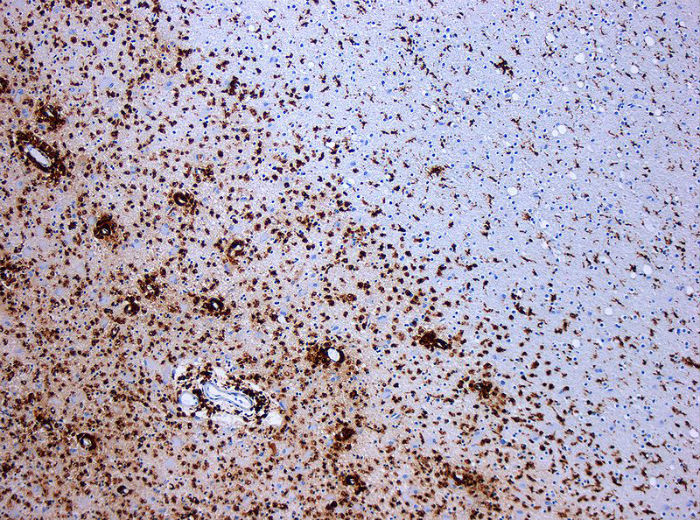
Demielinizare produsă de scleroza multiplă. Țesutul colorat cu CD68 evidenţiază mai multe macrofage în zona leziunii.
Scara original 1:100.
Sursa: Marvin 101/Wikipedia
Tratamentul pacienților cu scleroză multiplă [SM] este unul complex, medicamentele utilizate având diferite mecanisme, forme de administrare variate, intervale de administrare scurte sau lungi și, bineînțeles, efecte secundare care aparțin unei anumite clase de medicamente.
Medicamentele disponibile în 2024 și care vor continuă să fie utilizate și în 2025 sunt rezumate la sfârșitul articolului, precizând mecanismul de acțiune, modul de administrare, efectele secundare și compatibilitatea cu sarcina și alăptarea.
Anul 2024 a fost marcat de numeroase studii, unele pozitive, altele negative, dar pentru 2025 nu se așteaptă apariția pe piață a unor noi medicamente, întrucât procesul de aprobare a unei noi molecule este de lungă durată.
Cea mai importantă întâlnire științifică din domeniul SM, congresul ECTRIMS (European Committee for Treatment and Research în Multiple Sclerosis) a avut loc anul acesta în Copenhaga în perioada 18-20 septembrie 2024. O noutate majoră este propunerea actualizării criteriilor de diagnostic pentru scleroză multiplă, dar, pentru pacienți, două studii au o relevanță majoră din punctul meu de vedere, studiul HERCULES1 care a analizat medicamentul tolebrutinib la pacienții cu scleroză multiplă secundar progresivă și un studiu2 cu privire la suplimentarea cu doze mari de vitamină D la pacienții nou diagnosticați cu sindrom clinic izolat (CIS în engleză – clinically isolated syndrome), un precursor al sclerozei multiple.
Tolebrutinib, un inhibitor oral al tirozin kinazei Bruton (BTK), este primul medicament care a demonstrat că încetinește progresia handicapului la pacienții cu scleroză multiplă secundar progresivă fără puseu (nrSPMS). În studiul de fază3, numit HERCULES, medicamentul a redus cu 31% riscul de progresie a handicapului la 6 luni și aproape a dublat procentul de ameliorare a invalidității de la 5% la 10%, comparativ cu placebo. Cu toate acestea, medicamentul este asociat cu un risc de toxicitate hepatică, cu cazuri severe raportate la 0,5% dintre pacienți.
Tolebrutinib vizează inflamația de la nivelul creierului, în rândul pacienților cu nrSPMS care nu mai răspund la imunomodulatoarele tradiționale. În ciuda impactului său asupra progresiei handicapului, acesta nu a încetinit atrofia cerebrală, o constatare neașteptată. Sunt planificate cereri de reglementare pentru acest medicament, dar este puțin probabil ca medicamentul sa apară pe piață in 2025, întrucât sunt necesare cercetări suplimentare pentru a optimiza siguranța, în special în ceea ce privește toxicitatea hepatică.
Cel de-al doilea studiu a investigat efectele suplimentării cu doze mari de vitamina D la pacienții nou diagnosticați cu sindrom clinic izolat (CIS), un precursor al SM. Studiul a inclus 303 participanți, predominant femei, cu niveluri serice inițiale de vitamina D sub 100 nmol/L. Pe parcursul a 24 de luni, participanții au primit 100 000 UI de colecalciferol sau placebo la două săptămâni, activitatea bolii (recidive, leziuni noi / lărgite și leziuni active) fiind rezultatul primar al studiului.
Rezultatele au arătat o reducere relativă de 34% a activității bolii în grupul cu vitamina D comparativ cu placebo, cu un timp median până la activarea bolii ce a fost aproape dublat (432 vs. 224 de zile) față de cei tratați cu placebo. Nu au fost înregistrate efecte adverse semnificative sau semne de hipercalcemie. Cu toate acestea, nu s-au observat îmbunătățiri în ceea ce privește ratele de recidivă, progresia handicapului sau calitatea vieții.
Acest studiu sugerează că dozele mari de vitamina D reprezintă un potențial tratament suplimentar, sigur și eficient pentru SM „precoce”, justificând studii suplimentare. Cercetătorii au observat că durata mai lungă a studiului și designul robust au contribuit probabil la succesul său în comparație cu cercetările anterioare3 care au avut rezultate contrastante.
Revenind la tratamentele disponibile în prezent, ultimul medicament aprobat în Europa este Kesimpta (ofatumumab) care a primit autorizația de punere pe piață din partea AEM (Agenția Europeană a Medicamentului) în primăvara anului 2021. În ultimii 2-3 ani, numeroase studii au confirmat siguranța utilizării noilor medicamente atât în sarcină, cat și alăptare.
Mai jos sunt prezentate medicamentele disponibile pentru tratamentul sclerozei multiple în Europa și implicit în România. Medicamentele rar utilizate precum alemtuzumab (Lemtrada), mitoxantrone (Novantron), siponimod (Mayzent), ponesimod (Ponvory), peginterferon beta-1a (Plegridy) nu sunt prezentate, dar pot fi consultate pe diferite site-uri ale societăților de scleroza multipla: MS Society si National MS Society.
Informațiile provin din diferite surse (recomandări internaționale si naționale), site-ul Agenției Europene a Medicamentului, studiile pentru punerea pe piață a medicamentelor.
În ciuda efector secundare prezentate în tabel, trebui ținut cont de faptul că majoritatea pacienților tolerează foarte bine noile medicamente și doar o mică parte prezintă efecte secundare grave, cu rezultate excelente pentru noile molecule și o viață aproape normală pentru mulți pacienți.
Privind sarcina și alăptarea, recomandările sunt diferite în Europa și se bazează fie pe studii ce au fost efectuate după lansarea pe piață a medicamentelor, fie pe experiența centrelor experte (Franța, Germania, Italia, țările nordice) sau a recomandărilor unor societăți savante. Un medicament care este utilizat în Germania și Elveția în timpul sarcinii este posibil să fie interzis în Franța, Italia și România. Atât în Franța, cat și în Elveția, natalizumabul este folosit în alăptare fără nicio restricție, cu toate că medicamentul nu este autorizat în alăptare. Un alt foarte bun exemplu este rituximabul care este folosit în țările nordice cu rezultate foarte bune în ciuda faptului că medicamentul nu este aprobat pentru scleroză multiplă4.
Substanța activă (denumire comercială): acetat de glatiramer (Copaxone)
Mecanism de acțiune: nu este cert; se presupune că un peptid mimează proteine de la suprafața mielinei si saturează limfocitele (un fel de vaccin)
Mod de administrare: injectabil subcutanat; o data sau de trei ori pe săptămână in funcție de dozaj
Efecte secundare: nu exista efecte grave, doar benigne si tranzitorii. Poate produce lipodistrofie la locul de injectare (reacție imuna la injecție în apropiere de locul injectării, care apare ca o scobitura neestetica în țesutul grăsos) si necroza cutanata
Compatibil cu sarcina: da
Compatibil cu alăptarea: da
Substanța activă (denumire comercială): interferon β (Avonex/Rebif)
Mecanism de acțiune: citokina cu activitate antiinflamatorie
Mod de administrare: injectabil intramuscular; o data pe săptămână
Efecte secundare: simptome asemănătoare sindromului gripal; poate produce lipodistrofie si necroza cutanata. Rar: anemie, limfopenie (scăderea numărului de limfocite), afectare hepatica, depresie
Compatibil cu sarcina: da
Compatibil cu alăptarea: da
Substanța activă (denumire comercială): teriflunomide (Aubagio)
Mecanism de acțiune: inhibă proliferarea limfocitelor T si B active prin inhibarea pyrimidinei
Mod de administrare: oral, 1 comprimat pe zi.
Efecte secundare: căderea parului, limfopenie, afectare hepatica
Compatibil cu sarcina: nu este aprobat în sarcină din cauza efectelor teratogene observate în studiile preclinice și pentru că există alternative sigure.
Compatibil cu alăptarea: idem sarcina
Substanța activă (denumire comercială): dimethyl fumarat (Tecfidera) și diroximel fumarat (Vumerity)
Mecanism de acțiune: reduce activarea si proliferarea limfocitelor T si B; activează semnalizarea Nrf2 care reglează răspunsul celular la stresul oxidativ reducând inflamația cronica
Mod de administrare: oral, 1 comprimat de 2 ori pe zi.
Efecte secundare: dureri abdominale, bufeuri de căldura, diaree, greață, limfopenie, afectare hepatica, reacție alergică; in cazuri rare LEMP (leucoencefalopatie multifocală progresivă)
Compatibil cu sarcina: poate fi folosit dacă pacientul este deja sub tratament cu Tecfidera, dar nu se va începe tratamentul dacă sarcina este planificată sau dacă pacientul este pe un alt tratament contraindicat în sarcină.4
Compatibil cu alăptarea: idem sarcina
Substanța activă (denumire comercială): fingolimod (Tysabri)
Mecanism de acțiune: blocarea limfocitelor în ganglionii limfatici
Mod de administrare: oral, 1 comprimat pe zi.
Efecte secundare: bradicardie (scăderea frecvenței cardiace – la inițierea tratamentului), hipertensiune arteriala, risc de infecții (in special veruci plantare si alte infecții cu papilomavirusul uman), herpes, zona zoster, cancer de piele si ginecologic, edem macular, hepatita medicamentoasa, rar LEMP
Compatibil cu sarcina: nu este aprobat in sarcina din cauza efectelor teratogene observate in studiile preclinice si pentru ca exista alternative.
Compatibil cu alăptarea: idem sarcina
Substanța activă (denumire comercială): cladribina (Mavenclad)
Mecanism de acțiune: reducerea limfocitelor prin citotoxicitate
Mod de administrare: oral, in funcție de greutate se ia tratament timp de o săptămână, se repeta după 1 luna si același regim se repeta după un an; practic 4 săptămâni timp de 2 ani.
Efecte secundare: infecții (in special zona zoster), greață, scăderea numărului de limfocite, risc de cancer
Compatibil cu sarcina: nu este aprobat in sarcina din cauza efectelor teratogene observate in studiile preclinice si pentru ca exista alternative. Preconcepția este autorizata la 6 luni după ultima doza.
Compatibil cu alăptarea: nu se alăptează timp de o săptămână după ultima doza.
Substanța activă (denumire comercială): natalizumab (Tysabri)
Mecanism de acțiune: acționează împotriva anti-integrinei α4 , împiedicând traversarea barierei hematoencefalice
Mod de administrare: injectabil intravenos (perfuzie), o perfuzie la 4-6 săptămâni (diferă in funcție de tara si stadiul tratamentului) sau injectabil intramuscular, 2 injecții in același timp la un interval de 4 săptămâni (in prezent se studiază intervalul de 6 săptămâni)
Efecte secundare: urticarie, durere de cap, creșterea numărului de eozinofile, creșterea numărului de leucocite. Tratamentul poate deveni ineficient se dezvolta anticorpi împotriva medicamentului.Risc de recidiva la întreruperea tratamentului. Dar efectul redutabil este dezvoltarea LEMP
Compatibil cu sarcina: da, cu un foarte bun profil de securitate in sarcina, dar intervalul la care se efectuează perfuziile se mărește la 6 săptămâni, iar tratamentul se oprește de obicei in trimestrul al III-lea.
Compatibil cu alăptarea: da
Substanța activă (denumire comercială): ocrelizumab (Ocrevus)
Mecanism de acțiune: anticorp monoclonal care țintește limfocitele B CD20
Mod de administrare: injectabil intravenos (perfuzie), o perfuzie la 6 luni; primele doua perfuzii se fac la un interval de 2 săptămâni; după 2 ani de tratament se poate discuta prelungirea intervalului dintre doze
Efecte secundare: risc crescut de infecții (in special pneumonie, infecții urinare, herpes) prin scăderea imunoglobulinelor, reacții la perfuzie, hipertensiune arteriala; căderea părului la anumite persoane, risc de cancer pe termen lung
Compatibil cu sarcina: poate fi folosit in sarcina doar in cazurile severe.
Compatibil cu alăptarea: ultimele studii demonstrează ca alăptarea este sigura daca medicamentul este indicat din cauza severității bolii.
Substanța activă (denumire comercială): ofatumumab (Kesimpta)
Mecanism de acțiune: anticorp monoclonal care țintește limfocitele B CD20
Mod de administrare: injectabil subcutanat, o injecție pe luna; in prima luna se vor efectua 4 injecții
Efecte secundare: risc crescut de infecții, dureri de cap, reactivarea hepatite B
Compatibil cu sarcina: idem Ocrevus
Compatibil cu alăptarea: idem Ocrevus
Substanța activă (denumire comercială): rituximab (Mabthera)
Mecanism de acțiune: anticorp monoclonal care țintește limfocitele B CD20
Mod de administrare: injectabil intravenos (perfuzie), o perfuzie la 6 luni; primele doua perfuzii se fac la un interval de 2 săptămâni; după 2 ani de tratament se poate discuta prelungirea intervalului dintre doze Folosit in special in tarile nordice întrucât nu este un medicament aprobat in tratamentul SM
Efecte secundare: risc crescut infecții, reacții la perfuzie, risc de sângerare prin scăderea numărului de trombocite, risc de cancer pe termen lung
Compatibil cu sarcina: nu este aprobat in sarcina. In cazuri severe a fost utilizat in boli reumatologice cu efecte secundare la unii copii.
Compatibil cu alăptarea: nu este aprobat in alăptare cu toate ca prin extrapolare de la ocrelizumab se poate considera un medicament sigur.
Bibliografie
1. https://www.sanofi.com/en/media-room/press-releases/2024/2024-09-02-05-00-00-2938875
2. ECTRIMS 2024 Abstract Number: 1291/O065 High-dose cholecalciferol reduces multiple sclerosis disease activity after a clinically isolated syndrome : results High-dose cholecalciferol reduces multiple sclerosis disease activity after a clinically isolated syndrome : results of a 24-month placebo-controlled randomized trial of a 24-month placebo-controlled randomized trial (D-lay MS D-lay MS)
3. Butzkueven H et al. Vitamin D did not reduce multiple sclerosis disease activity after a clinically isolated syndrome. Brain 2023 Dec 12
4. Hellwig K, Rog D, McGuigan C, et al. Final analysis of 379 pregnancy outcomes after exposure to dimethyl fumarate in a prospective international registry. Multiple Sclerosis Journal. 2024;30(2):209-215. doi:10.1177/13524585231220232
